近日,化学与材料学院王成明教授课题组首次采用氮杂环卡宾(NHC)催化,通过单电子转移(SET)途径,设计了分子间Heck-型烷基自由基加成诱发的分子内环合反应,高效实现了对含有季碳中心吲哚酮类化合物的构筑。相关研究工作发表在国际知名期刊Org. Lett.上,暨南大学王成明教授和中南民族大学孙焕博士、刘吉开教授为论文的共同通讯作者。
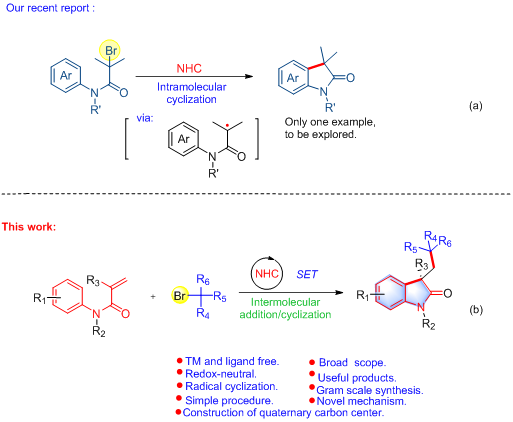
图1. NHC-催化含季碳中心的吲哚酮合成
很多天然产物和药物分子中均含有3,3’-二取代的吲哚酮结构,因此开发多样性的合成这类骨架的方法具有重要意义(图2)。由于季碳中心的构筑通常存在空间位阻问题,这类化合物的构建仍存在不小的挑战。目前含季碳中心的吲哚酮的合成主要通过过渡金属催化实现,具有:反应条件苛刻、选择性差、代价高、毒性大等缺点。因此,发展非金属催化,可持续、绿色、清洁的含季碳中心吲哚酮的合成方法十分必要和迫切。
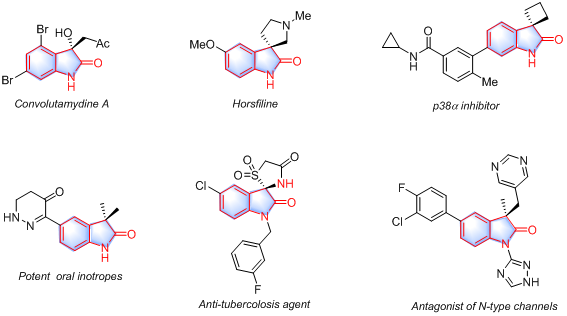
图2. 含3, 3’-二取代吲哚酮骨架的生物活性分子
另一方面,N-杂环卡宾 (NHCs) 在有机合成、配位化学、和材料科学中有着广泛的应用。然而,N-杂环卡宾的化学应用很大程度上局限于醛或其它含有活性羰基官能团的底物 (如:酰氟或a,b-不饱和酯)。进一步探索和开发N-杂环卡宾新颖的反应机制,将底物的适用范围扩大到传统的醛类之外,对这一研究领域具有十分重要的意义。
近期,王成明教授课题组刚刚报道了第一例NHC-催化无醛类底物参与的a-溴代芳基酰胺的分子内自由基环合反应(图1,a),在很大程度上拓宽了N-杂环卡宾的化学(Org. Chem. Front. 2021, 8, 1454–1460)。本文是在上述研究基础上,王成明教授课题组在这一领域的进一步深入研究。
研究工作表明:该反应具有良好的官能团兼容性和催化效率,且操作简便,并可以顺利地放大到克级反应,进一步拓宽了这一发现的实际应用价值。
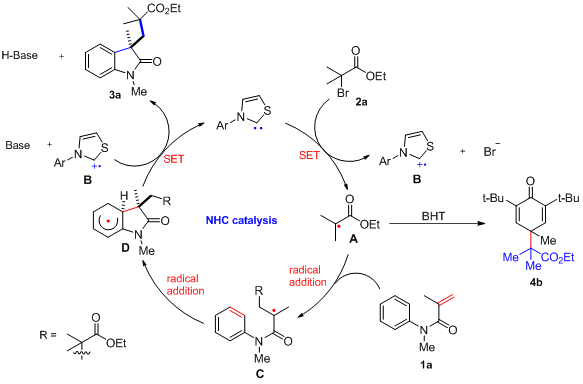
图3. 可能的反应机理
最后,作者还进一步研究了这一反应的可能机理(图3):N-杂环卡宾作为单电子还原剂和催化剂,向a-溴代羧酸酯提供一个电子,从而产生NHC自由基阳离子中间体B和相关的a-碳自由基A,作者通过自由基捕捉实验证明了这一点。自由基A加成到碳–碳双键上会生成碳自由基C,然后碳自由基C迅速进行另一次分子内自由基加成,形成中间体D。随后,碱进一步促进均相芳香取代反应顺利发生,并进行第二次SET过程。伴随着D的去质子化,得到具有季碳中心的吲哚酮产物,并完成催化循环。
该研究工作得到了中央高校基本科研业务费,暨南大学学科建设优秀青年骨干项目,暨南大学引进人才启动经费的资助。
论文链接:https://pubs.acs.org/doi/abs/10.1021/acs.orglett.1c01400